高端 聯亞 國產疫苗懶人包 第二期結束就緊急授權可行嗎?



我從半年前就看到國產疫苗打算做完第二期就緊急使用授權(EUA)這個問題了,因為法規單位早在之前就要決定我們國產新冠疫苗的臨床試驗應該要怎麼進行,該看哪些資料,這都是之前就已經規劃好要這樣做的了。當時認為台灣沒有疫情,沒有執行第三期臨床試驗的環境,因此訂出了這樣擴大二期的作法,將第二期收到三千人以上,想多看一些安全性,有效性則期待用中和抗體效價來解決。但這樣的擴大二期能不能取代國外第三期臨床試驗能看到的事情?我想這裡就很見仁見智了,醫界藥界的一些老師們其實也都有發出他們的憂慮之聲。
我原本預期這個議題會在六月高端聯亞的二期臨床試驗報告出來時才開始發燒的,沒想到現在因為國內社區疫情發生,而提早開戰。這篇就來整理一下吧。
寫在前面:
我沒有要黑國產疫苗的意思。我也衷心希望國產疫苗發展成功,能解決問題。但目前規劃做完三千人的第二期就送EUA,的確有很多學界師長們都憂心忡忡。我只是想點出這點。
台大醫院臨床試驗中心主任 陳建煒
台灣疫苗進度落後沒面子?國產疫苗不要急著上路!(2021.3.9)
https://forum.ettoday.net/news/1933514
國產疫苗是否有效需要實證數據 控制疫情不能靠妄想(2021.6.1)
https://forum.ettoday.net/news/1995597
謝炎堯教授:自由廣場》請陳時中慎思行政、法律責任(2021.2.17)
https://talk.ltn.com.tw/article/paper/1431614
涂醒哲老師:認購1000萬劑國產疫苗恐浪費公帑!涂醒哲:應以「台積電模式」開展台灣疫苗產業(2021.2.22)
https://www.businesstoday.com.tw/article/category/183027/post/202102220020
黃立民老師:國內疫苗最快6月獲緊急授權 專家擔憂沒有第三期數據、恐缺乏競爭力(2021.3.23)
https://news.pts.org.tw/article/518383
新冠疫苗的問題,當然專家們可能會有不同的意見,有老師覺得做完第二期就EUA是沒問題的,這是人數故意已經加多的第二期,應有一定參考性。次單位蛋白疫苗安全性應該還好等等。但也有人期期以為不可。我想這都可以討論,但我覺得討論基礎不能偏離事實。
疫苗臨床試驗是比較專業的東西,建議大家聽專業的發言即可,不要看一些奇奇怪怪帶風向昧於事實的消息。我拜託大家了。
也請參考高端臨床試驗總主持人:台大謝思民老師的說法。
延伸閱讀:
也來些正方代表的說法供大家參考:
疫苗緊急使用授權條件 怎樣才符國家利益(陳志榮、林奏延)(2021.4.5)
國產疫苗vs.國外疫苗 李秉穎對國產疫苗提6點 (2021.6.1)
高端疫苗第二期臨床試驗的計畫
https://www.clinicaltrials.gov/ct2/show/NCT04695652
聯亞疫苗第二期臨床試驗的計畫
https://clinicaltrials.gov/ct2/show/NCT04773067

2021.6.10 食藥署剛剛已經公布了詳細的國產新冠疫苗緊急使用授權審查標準。
我來劃重點,這次新增的主要是療效評估標準的部分。
所附臨床試驗報告需有接種試驗疫苗受試者至少3000人於接種最後一劑疫苗後至少追蹤1個月,且所有受試者於接種最後一劑疫苗後追蹤時間中位數至2個月的累積安全性資料,並須包含65歲以上特殊族群之試驗結果。

1.高端下午要解盲,你早上公布EUA詳細標準。好吧,總比不公布好,但這個公布時機難免會招人批評。你想像一下,如果美國FDA在輝瑞公布期中報告那天的上午才公開公布他們的詳細EUA審查標準,美國學界會不會暴動?
2.我能體會食藥署也盡力了,去年10月公開簡單的標準,但一直沒有把詳細針對療效要怎麼評估標準寫出來。原因也很簡單,因為WHO一直遲遲沒有訂出標準。如果國際已經有免疫橋接測中和抗體的指引訂出,那我們就解套了,但問題就是還沒有訂出來呀。
3.我想現在是因為我們審查EUA在即,只好硬著頭皮公布這個詳細標準了。但我相信這個方向規劃已久,廠商大概也都知道方向,因為食藥署三月就委託部立醫院蒐集200位國人接種AZ疫苗之中和抗體結果作為外部對照組,五月初起陸續召開專家會議討論,研商以免疫橋接(immuno-bridging)方式,採用免疫原性(中和抗體)作為替代療效指標,看國產疫苗產生的抗體是否和國外已經EUA的AZ疫苗相當,作為支持國產疫苗療效的佐證。
4.這個方法也寫得很小心,寫如果申請EUA前WHO訂出了國際的中和抗體保護力相關指標閾值,則參考WHO的標準。
5.簡單來說,國產疫苗二期臨床試驗所得中和抗體效價必須證明不能比AZ差,才會EUA。
6.但一切重中之重的問題還是,免疫橋接是很可能會進行的方向,但在此刻WHO的確沒有訂出標準。如果在我們審查是否要給予兩個國產疫苗EUA之前,國際標準都沒有公布,那這就是台灣自己訂的不一定能和國際接軌的標準。這會引起很大的爭議。
2021.6.10 COVID-19國產疫苗信任危機走火關鍵──比臨床試驗更需要「解盲」的決策過程
2021.6.2
我和何美鄉老師在公視有話好說針對這個議題的討論。留言區有網友:陳亮宇整理了時間軸,大感謝!
01:00 疫情現況報告
04:30 來賓分析疫情趨勢 (林氏璧:過去資料塞車導致校正回歸,但是陽性案例已優先登打,尚未登打的案例以陰性為主,校正回歸應該不多了)
05:50 台灣防疫策略要升級清零或延續現有策略? (何美鄉:考慮疫苗即將抵台,沒有必要升級追求清零;但是降級需要更多的數據支持)
13:37 疫苗延遲交貨原因 (何美鄉:莫德納延遲原因不明,AZ是因為全球產量不足, COVAX 平台是以疫情嚴重程度配送疫苗,台灣疫情相對不嚴重)
20:25 林氏璧:美國要求疫苗必須被人民接受, 輝瑞/BNT, 莫德納跟嬌生都有做數萬人的三期臨床測試,收案後進行第一階段分析,依照分析結果核准緊急授權 EUA 。
26:47 臨床測試介紹 (何美鄉:臨床第二期只要求呈現抗體數量,不用到疫區分析感染狀況;臨床第三期要求感染分析,必須到疫區進行)
28:50 如何驗證疫苗安全性? (何美鄉:通常必須經過兩年追蹤,但是現況不允許)
29:17 國產疫苗現況 (依照節目資料,台灣兩支疫苗都有國外三期臨床實驗計畫,但是要做到 2020 年底)
32:07 WHO 正在探討二期臨床後核發 EUA 的可行性 (何美鄉:這個方法是參考流感疫苗,導入先上市的疫苗數據減少後上市的疫苗驗證過程。因為流感疫苗長期受到監控,標準檢驗試劑完備,肺炎病毒目前沒有標準試劑,改為綜合比較復原者和先上市疫苗施打後產生的抗體)
39:45 台美 EUA 標準比較:
美國要求「三期」測試三千人,至少追蹤一個月,台灣要求「二期」測試三千人,至少追蹤一個月。
美國規定要有 50% 有效性 (何美鄉:台灣「現在的」疫情不足以進行有效性驗證)
44:50 台灣的 EUA 標準能否說服兩位來賓?
林氏璧:蛋白疫苗的安全性的確很高,佐劑的副作用也很清楚;但這終究是一支全新的疫苗,是否會產生意料之外的變化,有一點點擔心。
何美鄉:因為對安全性沒有疑慮所以願意去當白老鼠 (何美鄉跟陳建仁都有參與國產疫苗二期人體試驗) ,有效性部分,依照現有科學證據,應該可以用比較抗原的替代三期驗證;當然,有進行三期更好。
這個podcast中幫大家整理了李秉穎老師和何美鄉老師的說法。看不懂有話好說中何老師的說明者,讓我來說給你聽!
國產第二期可EUA的贊成方說法 李秉穎 何美鄉篇 以中和抗體反應有效性
https://linshibi.pros.is/3hnx84
這個podcast中幫大家整理了三位陳老師的說法,請參考!
國產疫苗第二期可EUA的正反方說法 陳建仁 陳建煒 陳培哲篇
https://linshibi.pros.is/3j5zdw

疫苗臨床試驗中和抗體的效價到底可否作為有保護力的替代指標呢?Nature Medicine一篇文章分析了七個疫苗各自和康復者抗體的比例來訂出一個預測的模型。
論文:Neutralizing antibody levels are highly predictive of immune protection from symptomatic SARS-CoV-2 infection
https://www.nature.com/articles/s41591-021-01377-8
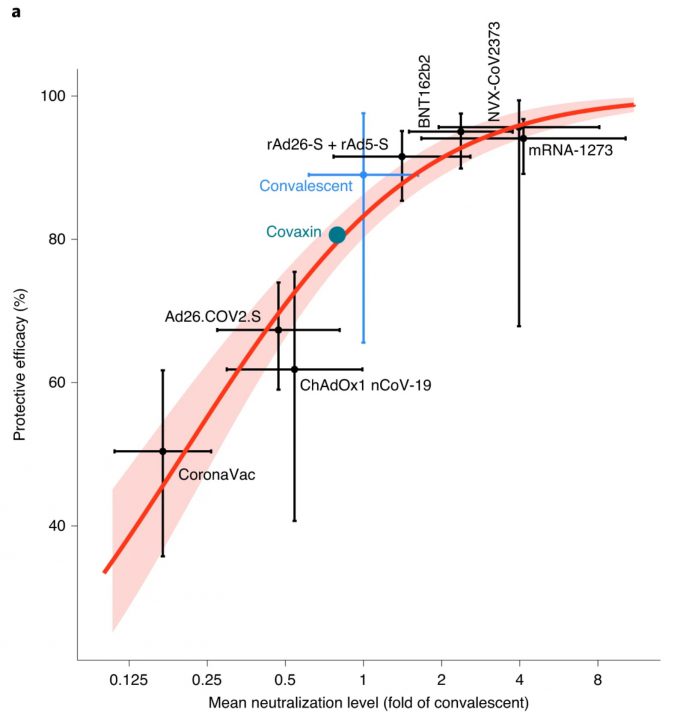
他們估計如果可達到康復者中和抗體的 20.2%就可達50%的保護力,估計如果可達到康復者中和抗體的 3%就可防重症。
WHO前陣子也開了會,研討免疫橋接研究替代第三期臨床的可能性。我想大方向是這樣的沒錯,希望WHO早日有共識。畢竟目前的階段再進行原本第三期完全安慰劑對照組的臨床試驗的確是有醫學倫理的疑慮。但如果要和已EUA的疫苗兩兩比較,又曠日費時,有些不切實際。
2021.5.30
國產疫苗最近吵翻天,我來澄清三個問題。
1.國外疫苗也沒有做完第三期就緊急使用授權(EUA)呀!那國產疫苗只做完第二期就EUA有什麼問題嗎?
A:國外新冠疫苗的EUA,我在podcast中講太快說國外是做完第三期才EUA,對,我口誤了。但聽我完整說明應該都聽得出來,我指的是”第三期做到一定程度給EUA”,以美國FDA是做注射疫苗萬人以上的第三期,打完第二劑,有平均兩個月的追蹤後才能送件EUA。
輝瑞/BNT,莫德納,嬌生,AZ皆如此,有了第三期的初步報告,才給EUA。
整個第三期要完全收尾,還需要長期追蹤。這些臨床試驗須要追蹤兩年,比方說輝瑞的計畫到2023年的4月6日才會結束這整個研究。當然不會等到”做完”才EUA。
我們是二期做完就想要EUA,完全不一樣。
我說過多次了,全世界這一年來做完第二期就直接EUA的,只有中國和俄羅斯兩國。當然他們的第二期人數都比較少,不到一千人。我們的第二期有故意增加人數到3000人。但這樣能不能取代第三期?我想這裡就很見仁見智了。
2.那國產疫苗這樣直接EUA會有安全性和有效性的問題嗎?
A:我個人認為只看3000多人的安全性就EUA是不夠的。因為你會漏掉五千分之一,萬分之一這樣的副作用。
國外為何要看萬人以上,且要追蹤兩個月不是隨便規定的。那都有他想看到的重要疫苗副作用。
你可以說,如AZ產生10萬分之一的TTS血栓問題,這萬人臨床試驗也無法偵測出來呀。這無法說服我。十萬分之一罕見的副作用偵測不到,不能作為你跳過第三期的理由。
3.可是2009年國光的H1N1流感疫苗也沒有做第三期呀?
A:流感已經研究多年,早已確認抗體的效價可以當作有效性的替代指標(Surrogate Marker),有一定的抗體就可以視為這疫苗是有效的,不需要做第三期。
而流感疫苗平臺早已成熟,只是替換其中的病毒株,安全性也經過長久的驗證。
新冠疫苗是新的疫苗,目前國際上還沒有訂出標準說多少抗體的效價是否就可以界定為有效,兩者完全不能類比。即使你做疫苗的平台是原本就有的,但你這疫苗還是全新的呀。可能會有未知的副作用產生。
4.國內已有疫情,高端聯亞是否可在台灣做第三期?對照組是否應該用另一個疫苗,而不是食鹽水安慰劑?
是的,如果要在台灣做第三期,目前在國際已經有確認有效的疫苗狀況下,對照組完全用安慰劑是有醫學倫理上的問題的。因此,有可能對照組需要用另一個疫苗,比方拿AZ疫苗來當對照,證實效果不會比AZ疫苗差。

2020.9.6更新:台灣的聯亞生技還有高端疫苗都在8月底前得到了食藥署有條件核准其第一期臨床試驗計畫,兩者皆有望在九月開起第一期臨床試驗。
食藥署有條件核准聯亞生技開發股份有限公司COVID-19候選疫苗之第一期臨床試驗計畫
食藥署有條件核准高端疫苗生物製劑股份有限公司COVID-19候選疫苗之第一期臨床試驗計畫
台灣聯亞生技(United Biomedical, Inc.,Asia)的UB-612疫苗「UB-612(S1-RBD-sFc, Th/CTL Peptides)」是屬於次單位疫苗,預計在中國醫藥大學附設醫院進行第一期臨床試驗,試驗主持人為黃高彬主任,預計收60人。
以下是新聞稿:
UBI/聯亞集團所研發之高精準設計COVID-19疫苗UB-612獲台灣衛福部有條件核准進行第一期臨床試驗
聯亞生技今日宣佈,台灣衛生福利部食品藥物管理署(TFDA)有條件核准UBI/聯亞集團所研發之高精準設計COVID-19疫苗UB-612進行第一期臨床試驗,聯亞生技將開始篩選合格受試者,待於九月初完成補件並取得正式核准後,開始施打疫苗。本試驗將於健康成人受試者施打兩劑UB-612疫苗,受試者分低、中、高三個劑量組,每組20位,預計共收60位,主要目的為探索本疫苗之安全性、耐受性及免疫原性。試驗醫院為中國醫藥大學附設醫院黃高彬主任擔任試驗主持人。
聯亞生技表示,UB-612疫苗係UBI/聯亞集團利用其獨有之專利平台技術,針對SARS-CoV-2病毒開發之高精準設計疫苗(high precision designer vaccine)。UB-612除了含有精準設計之S1-RBD病毒抗原外,更加入了全球首創之CTL及Th抗原決定位胜肽,這些胜肽選自於可與人類MHC I和II結合且具免疫優勢之M、S2和N部位。此經過精準設計之Th/CTL混合胜肽可以活化T細胞,並引發T細胞之記憶反應和效用功能。在動物試驗中,注射UB-612疫苗除了使動物產生大於10,000倍稀釋之高度特異性中和抗體(遠高於目前國際間任何COVID-19疫苗),亦可產生Th1型之T細胞免疫反應。預期具多重成分之UB-612疫苗於人體將能引起均衡之B細胞活化並擴大T細胞免疫反應,以達到良好保護效果。
基於以上非臨床試驗結果,UB-612疫苗已有條件獲准於台灣進行第一期臨床試驗,並規劃於台灣、美國及巴西等國進行第二/三期多國多中心臨床試驗,以證實疫苗之療效與安全性。UBI/聯亞集團已在台灣建立TFDA及美國FDA核准之生產設施,並計劃在2020年12月至2021年第一季間於集團內公司生產5,000萬至1億劑疫苗,2021年則可在無需委外之情況下生產5至10億劑,使得未來定價極具成本效益之競爭性。

台灣的高端疫苗(Medigen Vaccine Biologics.)則與美國國衛院(NIH)合作,其疫苗「MVC-COV1901 vaccine(SARS-CoV-2 S-2P棘蛋白) Injection」是屬於次單位疫苗,預計在台灣大學附設醫院進行第一期臨床試驗,試驗主持人為謝思民老師,預計收45人。
臨床試驗詳情:
A Phase I, Prospective, Open-Labeled Study to Evaluate the Safety and Immunogenicity of MVC-COV1901
2021.5.14 首波國產疫苗備戰 高端、聯亞拚7月底供應
國內疫情本週急速升溫,總統蔡英文13日召開國安高層會議,會後談話表示預計7月底可以開始供應第一批國產疫苗。國產疫苗目前臨床進度方面,高端疫苗、聯亞生技可望領先量產,國光生技因策略上調整劑量、佐劑,二期臨床試驗略為落後。
國內疫情持續升溫,總統蔡英文指出,台灣向國外訂購的其他新冠疫苗,6月後會進入分批交貨期;至於國產疫苗可於7月底開始供應第一波疫苗。
目前國內疫苗廠商的研發進度,高端和聯亞在完成收案後,可望最快於6月初及6月中旬依法規申請緊急使用許可(EUA),並於7月底供應第一批國產疫苗。
高端的候選疫苗MVC-COV1901技轉自美國國衛院(NIH)的基因重組S-2P棘蛋白技術,並於2020年12月30日開始收案。
高端指出,二期臨床試驗已於4月底完成3800人施打,並依緊急使用許可(EUA)規範觀察成效和安全性1個月,預計5月底結束觀察期,並整理臨床試驗分析數據;若數據達到預期目標,最快6月初依法規申請緊急使用許可,待衛福部審查通過,有機會達成7月底出貨目標。
高端目前產能約200萬劑,將逐步擴大至300萬劑。至於疫苗抗原原液,目前仍由高端自行生產,未來緊急使用許可取得,將視疫苗訂單需求與台康生分配產能比例,估計年產能最大可達1000萬劑。
聯亞方面,預計測試者本週或最遲下週可打完第二劑;在第二劑接種後28天就能做抗體血清濃度測試,之後將測試統計結果送到食藥署,由食藥署進一步評估。若獲緊急使用授權,7月底即可開打。
產能方面,聯亞生技將與旗下子公司聯生藥、聯亞藥共同合作生產,其中聯生藥新竹總廠已通過歐盟GMP查核,後續將負責生產疫苗蛋白質原料藥;聯亞藥則有無菌針劑生產線。
至於國光生技武漢肺炎疫苗開發案,進度上略為落後,目前策略上將以增加抗原含量、配合佐劑來執行第二期臨床試驗,持續投入疫苗研發。
歡迎追蹤前台大感染科醫師。04b的發聲管道!
希望大家當我的種子教師,推廣正確的新冠衛教。
科學防疫,不要只以恐懼防疫!
林氏璧醫師的電子名片
https://lit.link/linshibi
每週一9PM直播解說疫情
https://www.youtube.com/user/linshibi
加入LINE@ 訊息不漏接
https://lin.ee/3uf7fpN
Telegram也很好用喔
https://t.me/linshibi
Instagram也有喔
https://www.instagram.com/linshibi/
我也有podcast了喔!
林氏璧孔醫師的新冠病毒討論會
https://linshibi.pros.is/3dclww
對這個病有較正確的認知遠比哪裡又多了案例重要!
新冠肺炎疫情下的防疫須知 常見問題解答FAQ
2019新型冠狀病毒懶人包 戴口罩勤洗手
冠狀病毒流感化?武漢肺炎疫情走向預測
新冠感染各國分年齡致死率整理 小於49歲致死率較低 小於19歲較不易染病
14天檢疫期滿後才確診?新冠潛伏期大於14天嗎?無症狀感染者的發病日和確診日?
變種病毒
新冠變種病毒懶人包 英國 南非 巴西 加州 菲律賓 日本 李秉穎:嗤之以鼻?
英國新冠變種病毒 傳染力增加70% 英國進入第四級封鎖 新冠疫苗還有效嗎?
台灣疫情
華航機師展開擴大採檢 添一本土案例是印尼機師之子 台北清真寺16日中午400人聚會
台灣首例醫師確診新冠 傳給護理師女友 院內感染還沒到院內群聚?
部立桃園醫院院內感染群聚事件懶人包 封院?清空?
台灣本土感染案771 紐西蘭籍機師航空器群聚感染一案整理
紐約時報評台灣防疫好運可以維持多久之我見:台灣的防疫絕不是只靠運氣
日本確診一例自台灣返日之新冠病毒無症狀感染者 南部讀書的日籍女學生
比利時工程師是台灣本土感染嗎?
彰化縣萬人血清抗體篩檢懶人包 台大公衛和彰化縣衛生局合作研究
專家意見
黃立民教授 新型冠狀病毒訪問共筆
張上淳教授共筆 中央流行疫情指揮中心記者會
李秉穎老師新冠病毒訪問共筆
西班牙流感 1918年流感大流行 別小看流行性感冒!
武漢肺炎發生率與致死率的國際比較 by 陳建仁副總統
治療經驗
新型冠狀病毒 武漢肺炎 COVID-19 治療經驗分享
新型冠狀病毒的抗病毒藥物治療 瑞德西韋 法匹拉韋 硫酸羥氯喹
瑞德西韋 remdesivir 新冠治療臨床試驗懶人包
類固醇可降低新冠重症死亡率
新冠病毒如同愛滋病毒會攻擊免疫系統?用類固醇就好了?
小心沉默的肺炎!日本自衛隊中央病院新冠治療經驗
疫苗進度
新冠疫苗懶人包:保護力 副作用 效力多久 疫苗護照 不同廠牌混打 一次回答你!
新冠疫苗進度 進入第三期臨床試驗的疫苗總整理
新冠疫苗爭奪戰 日本對新冠疫苗的超前佈署 台灣何時會有疫苗?COVAX會分配到什麼疫苗?
牛津疫苗懶人包:第三期臨床試驗結果整理 英國通過緊急授權
橫斷性脊髓炎是什麼?阿斯特捷利康和牛津大學合作的腺病毒新冠疫苗懶人包
AZ疫苗血栓之亂 歐洲多國停打 什麼是腦靜脈竇栓塞 瀰漫性血管內凝血 血小板下降?
莫德納(Moderna)的新冠疫苗:mRNA疫苗懶人包
輝瑞/BioNTech新冠疫苗懶人包:東洋破局 需要冷鍊的mRNA疫苗
俄羅斯史普尼克五號新冠疫苗懶人包 保護效力達92%
嬌生新冠疫苗懶人包 單劑保護力66% 南非變種病毒效力僅57%
嬌生疫苗血栓之亂 血栓併血小板低下症候群TTS懶人包
諾瓦瓦克斯(Novavax)次單位蛋白新冠疫苗懶人包 在英國保護力89.3% 南非變種病毒僅60%
世界疫情
美國新冠病毒疫情懶人包
英國佛系防疫的豪賭 陳時中:目前台灣沒有到那個情況 國家醫療量能無法承擔才會這樣做
東京有抗體者僅0.1% 大阪0.17%?世界各國新冠抗體陽性率 血清盛行率整理
日本再發布緊急事態宣言 首都圈1都3縣1月8日起採取緊急事態行動
東京面臨感染爆發重大局面 東京封城?首都封鎖?
東京第二波來了嗎?新冠七指標 東京警報(Tokyo alert)彩虹大橋紅色點燈
東京新冠病毒確診單日破百 小池呼籲避免到夜生活繁華街 東京監測指標修改
東京第二波疫情來襲 小池知事發布感染擴大特別警報
通天閣太陽之塔新冠紅綠燈 大阪府知事吉村洋文推出大阪模式
大阪府知事吉村洋文推薦優碘漱口水控制新冠病毒傳播 相關商品銷售一空
沖繩新冠疫情懶人包 沖繩美軍基地群聚感染
日本武漢肺炎 新冠病毒 COVID-19流行地圖
日本旅遊回來要被隔離14天嗎?可退費嗎?何謂旅遊疫情建議等級 流行地區分級?
台灣日本南韓新冠PCR檢驗量及陽性率比較 大阪 vs 北海道
鑽石公主號郵輪新型冠狀病毒疫情懶人包 由一個香港案例傳染給至少135人的海上悲劇




東京8805間旅館比價 京都7134間旅館比價
日本訂房請參考住宿懶人包,林氏璧推薦的二十四家東京旅館,26家大阪旅館,十三家京都旅館。
訂房網站推薦Relux,e路東瀛,Booking.com,Agoda。也可先用 旅館查價網站來看是否有便宜。訂行程網站推薦KKday,KLOOK客路。
到日本上網分享器和SIM卡的問題請看過這兩篇:2023日本上網卡 SIM卡懶人包,日本行動上網分享器懶人包。
各種毒友優惠及現在的活動請見:全日本篇,東京優惠,關西京阪神優惠,九州優惠,北海道優惠,沖繩優惠。
歡迎加入林氏璧的日本自助旅遊中毒者臉書粉絲專頁,或是小狸的日本購物血拼中毒者臉書粉絲專頁,接收最新日本旅遊訊息。近期有什麼活動會在粉絲專頁置頂,LINE官方帳號:@linshibi 則會直接發送最新的優惠訊息。
RSS訂閱/ 以Email訂閱 本站,東京訊息不漏接。
本站導覽 新手第一次到本站的導覽,比較容易找到資料喔。
重要公告 即日起本部落格(包括臉書頁面/私訊/e-mail)在非公開頁面不回答日本旅遊的常見問題,請各位見諒。請一律在日本自助旅遊中毒者臉書社團中問題讓大家集思廣益。
日本/東京自助旅遊的常見問題FAQ 新手請優先閱讀。




請教林醫師
國鼎生技的疫苗,如何呢?
國鼎生技宣布,旗下治療Covid-19的新藥二期期中數據通過美國數據監查委員會(DMC)審查,並建議擴大新增收治重症病患,預計第3季完成。若結果正向,將向美國FDA申請緊急使用授權(EUA)。
https://clinicaltrials.gov/ct2/show/NCT04773067
孔醫生您好,想詢問關於疫苗保護力的問題,在您的文章中有提到“不同臨床試驗做出來的保護力數字難以直接相比。因為做的國家,基本資料包括年齡層有無慢性病等,當地流行的病毒株還有流行狀況都不一樣。”許多專家也是如此說法,但Nature Medicine這篇文章預測的模型
畫出了不同臨床試驗中的中和抗體與保護力的線性關係,這樣是否表示不同疫苗的保護力在不同試驗中是可比的呢? 不知道孔醫師怎麼看