新冠疫苗懶人包 臨床試驗 疫苗何時會出來?


這篇會整理新冠病毒疫苗相關的新進展。 很多專家都期盼要等到疫苗真的做出來,才能真正解決這次新冠病毒的全球大流行,人類才能恢復原來的生活。美國國立過敏與傳染病研究院(NIAID)主任佛奇(Anthony Fauci)的推估是,疫苗需要12到18個月才能做出來。我個人的話會覺得新冠的藥物應該會比疫苗早出來,對疫苗我會偏保守看法而沒有這麼樂觀,因為目前為止沒有人類的冠狀病毒疫苗(針對SARS和MERS)被成功研發出來過,顯然技術上有遇到瓶頸。做一個疫苗曠日廢時,需要從體外試驗,動物試驗,到一系列的第一期,第二期,第三期的臨床試驗來證明其安全性和療效。任何一個步驟有問題,就前功盡棄沒辦法成功了。且就算有效疫苗問世被批准得以使用,還有後續的產能的問題,歐美研發的疫苗可能要先用於內需,台灣不一定能第一時間拿到。這些都是問題。
不過現在科技日新月異,全世界都在努力試著做出新冠的疫苗,台灣自己也在努力,我們還是能心存希望,也許我們真的能加速做出一個又有效又安全的疫苗,真正戰勝這隻頑強的病毒。
2020.5.18:莫德納(Moderna)的mRNA疫苗第一期臨床試驗初步結果公布後,股價應聲大漲24%
2020.5.19:波士頓環球報旗下媒體STAT的一篇質疑文章,又讓莫德納股價重挫。
2020.5.22:佛奇(Anthony Fauci)對於莫德納疫苗的第一期臨床試驗初步結果審慎樂觀。
2020.7.16:莫德納(Moderna)的mRNA疫苗第一期臨床試驗結果發表,第二期也完成,準備進入第三期
2020.7.20:英國和中國的第二期疫苗臨床試驗同日發表在刺胳針期刊
2020.7.31:日本和輝瑞藥廠達成合作協議,將於2021年6月前提供日本6000萬人份疫苗
2020.8.13:輝瑞藥廠/BioNTech共同開發的新冠mRNA疫苗第一/第二期臨床試驗結果正式刊登在Nature期刊
比較簡單進入第三期疫苗的表整理在這一篇
新冠疫苗進度 進入第三期臨床試驗的疫苗總整理
延伸閱讀:
紐約時報新冠疫苗整理網頁
WHO會更新全球疫苗進度 2020.8.13
疫苗研發的臨床參考要點
BBC中文網:全球各國新冠疫苗研發進展到了什麼程度 2020.4.20
BBC中文網:新冠病毒疫苗研發賽跑 盤點全球領先衝刺臨牀的六名「選手」 2020.5.5
國產新冠疫苗拚8月人體實驗 明春施打有望 1張圖看懂台灣進度 2020.7.17
疫苗新布局:爭取牛津授權、台廠代工有望,國家隊產能為何恐受影響? 2020.8.10
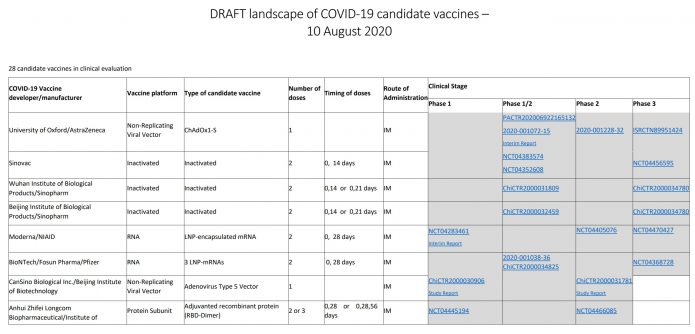
2020.8.13 目前最新進度:
世界衛生組織(WHO)8月13日發布全球新冠肺炎候選疫苗的研發進度整理,包括29個疫苗在臨床試驗中:6個疫苗在第三期臨床試驗、2個在第二期臨床試驗、21個在第一期臨床試驗(包括第一/第二期合併的),還有138個疫苗在臨床前試驗中,尚未進入人體試驗。
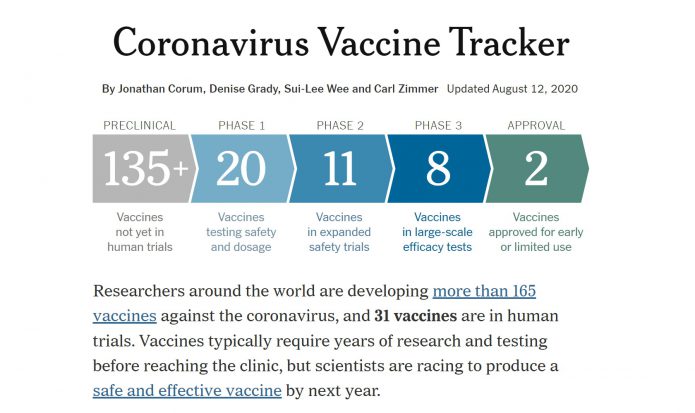
紐約時報則是整理至少有165個疫苗,包括31個疫苗在臨床試驗中:8個疫苗在第三期臨床試驗、11個在第二期臨床試驗、20個在第一期臨床試驗(以上第一/第二期合併的有重複計算),還有135個以上的疫苗在臨床前試驗中,尚未進入人體試驗。兩個已經緊急授權使用的,是俄羅斯還有中國康希諾生物的疫苗。
以下是幾個領先的疫苗:
1.英國阿斯特捷利康藥廠(AstraZeneca)和牛津大學合作的腺病毒疫苗「AZD1122」,第三期臨床試驗於6月15日開始收案,預計在巴西收案兩千人。
2.美國生物科技公司莫德納(Moderna)和美國國家衛生研究院(NIH)合作的mRNA疫苗「mRNA-1273」,第三期臨床試驗於7月27日開始收案,預計在美國收案三萬人。
3.德國生技藥廠BioNTech和美國輝瑞藥廠(Pfizer)合作的mRNA疫苗「BNT162」,第三期臨床試驗於7月27日開始收案,預計在美國,德國,阿根廷和巴西收案近三萬人。
4.中國北京科興生物( Sinovac)的減毒疫苗,和巴西公共衛生研究中心巴坦坦研究所(Butantan Institute)合作進行臨床試驗,第三期臨床試驗於7月21日開始收案,預計在巴西收案8870人。
5.中國國藥集團(Sinopharm)旗下武漢生物製品研究所研發的減毒疫苗,第三期臨床試驗於7月16日開始收案,預計在阿聯酋收案一萬五千人。
6.中國疫苗公司康希諾生物(Cansino Biologic)與軍事科學院合作研發的腺病毒疫苗「Ad5-nCoV」,第三期臨床試驗預計在沙烏地阿拉伯收案五千人。
2020.7.28 今日上廣播主題:「新冠疫苗新進展。台灣何時有疫苗?」
今天的題目比較困難,希望大家聽完能比較理解疫苗臨床試驗是怎麼回事喔!
美國Moderna疫苗 7月27日已經開始第三期,預計年底或明年初上市。
台灣指揮中心目前是決定臨床實驗只需做完第二期,就用緊急授權的方式讓大家施打,時間預計在2021年3月。我個人會覺得有點憂心就是了。因為第三期是驗證此疫苗是否真的有保護力的階段,且人數更多才能看到較稀有的副作用。
時間軸:
7:55 關於泰國移工:此刻無法排除是台灣本土感染
9:08 關於日本女學生:個人判斷是日本檢測的偽陽性
14:37 全世界疫苗研發現況
15:55 139個疫苗在前臨床階段
不好意思這裡說錯了,日本有一個疫苗進入第一期了!
日本研發新冠肺炎疫苗 首例人體臨床試驗
17:29 跑得快的不一定會撐到最後,疫苗的安全性還是重要的
19:23 佛奇對於年底或明年初有疫苗表達審慎樂觀,但上市到量產還有一段時間
20:38 各國疫苗介紹
23:01 第三期臨床試驗執行的方式
24:11 動物試驗介紹
26:06 第一期臨床試驗介紹
29:34 台灣疫苗進度 台灣民眾對臨床試驗接受度不似歐美
31:42 國外的疫苗台灣買得到嗎?
33:03 第二期臨床試驗介紹
34:00 第三期臨床試驗介紹
36:15 台灣目前沒有第三期的環境,指揮中心目前是決定臨床實驗只需做完第二期,就用緊急授權的方式讓大家施打,個人表示擔憂。因為第三期是驗證此疫苗是否真的有保護力的階段,且人數更多才能看到較稀有的副作用。
42:06 美國政府投資Moderna的mRNA疫苗10億美金
42:48 台灣疫苗預算:135億台幣,115億採購,20億研發疫苗
47:00 台灣疫苗研發面臨的困難
50:44 疫苗可以用技術授權自己製作嗎?
延伸閱讀:
我自己的直播中有臨床試驗結果比較詳細的解說,廣播上沒時間講細節!
Moderna的mRNA疫苗,27日順利開始收案了。預計在美國收三萬人,一半打疫苗一半安慰劑,看是否能有效預防感染。
美國政府多投資美金4.7億下去,總共投了10億了 2020.7.27
避免秋冬疫情一發不可收拾 陳時中:放寬疫苗臨床實驗標準 2020.7.8
新冠肺炎疫情秋冬再度爆發的隱憂籠罩下,中央流行疫情指揮中心決定,放寬國內疫苗研發門檻。指揮官陳時中今(8)日指出,為加速新冠病毒疫苗研發,臨床實驗只需進行至二期,人數限制也放寬。
陳時中強調,疫苗品質與風險一定要堅守,經過評估,不需要做到臨床三期,將改以臨床二期為標準,不論緊急授權或加速審查方式,都可以在臨床二期完成。此外,食藥署討論後也確定,將以國際上中等數目進行,選定實驗組1000千人、對照組300人,並請可生產到100萬劑疫苗的廠商盡快報價。
國內多家廠商積極研發新冠肺炎疫苗,但被前疾管局長蘇益仁等人質疑進度太慢,其中,食藥署成為箭靶,被批評墨守成規,例如第二期臨床試驗,國際間規定只需1500至2000人,但我國卻要求至少3000人,缺乏緊急授權,拖累疫苗研發進度,影響防疫成果。
聽到了醫界的質疑,陳時中除了宣布放寬疫苗研發相關規範,並透露,我國也持續和國外藥廠聯繫,關注國外疫苗引進,包括進口原液或爭取授權製造等方式。
食藥署吳秀梅署長專訪 2020.7.19
加速國產新冠肺炎疫苗研發 陳時中:每家最高獎勵5億元 2020.7.24
衛福部僅編20億研發預算 蔣萬安憂心資源不足 2020.7.24
中央流行疫情指揮中心指揮官陳時中今(22日)表示,政府已經編列好新台幣135億元預算。不過根據衛福部提供給立委蔣萬安辦公室的報告資料顯示,135億元疫苗預算中,115.5億元用來採購疫苗,研發經費則僅有20億元。蔣萬安表示,如果要從國外採購那現在接洽恐怕為時已晚,法規也還沒鬆綁,若是要國內研發投入的心力與資源也不足,讓人擔心會兩頭空。

2020.7.31:日本和輝瑞藥廠達成合作協議,將於2021年6月前提供日本6000萬人份疫苗
日本政府和輝瑞藥廠/德國公司BioNTech達成合作協議,如果疫苗成功開發並獲得主管機關授權的話,將於2021年6月前提供日本6000萬人份新冠mRNA疫苗。
輝瑞的疫苗需要施打兩劑,因此就是一億兩千萬劑的意思。此前英國已經訂了3000萬劑,美國訂了六億劑。
輝瑞表示可以和日本政府合作很光榮,在這麼困難的狀況下要舉辦東京奧運,可以成為幫助日本的力量,感覺很高興。希望臨床試驗可以成功,順利獲得主管單位許可,提供貢獻。
加藤大臣表示,之後會正式簽約合作。也和其他企業繼續交涉,希望能早日提供日本國人安全有效的疫苗。
輝瑞與德國公司BioNTech共同開發的新冠mRNA疫苗在七月公布了初步第一期/第二期臨床試驗的結果。類似Moderna的同原理疫苗,可以產生中和抗體,也有很好的Th1免疫反應。
在四個候選疫苗中,最後選定了BNT162b2來進行第二期/第三期臨床試驗,預計將收案三萬人,以多國多中心來進行,120個醫院遍布美國39州,還有阿根廷,巴西和德國。
若一切順利,輝瑞希望能在10月左右申請某些國家的緊急使用授權。他們預計在2020年底前提供一億劑,在2021年前提供13億劑。
NHK報導:新型コロナ ワクチン供給で米企業と基本合意 加藤厚労相
輝瑞新聞稿
首圖出自 STAT報導:Covid-19 vaccine from Pfizer and BioNTech shows positive results

2020.8.13更新:輝瑞藥廠/BioNTech共同開發的新冠mRNA疫苗第一/第二期臨床試驗結果正式刊登在Nature期刊
美國輝瑞藥廠與德國公司BioNTech共同開發的新冠mRNA疫苗(就是也有賣給日本的那個)的第一/第二期臨床試驗結果正式刊登在Nature期刊。
於5月4日開始收案,有45位18~55歲成人健康受試者參加,6月19日完成最後收案。受試者分為三組(每組15人),每組9人注射疫苗,3人為對照組注射安慰劑。注射的疫苗劑量各為10微克、30微克和100微克,注射完第一劑後,相隔21天再注射第二劑。
NHK報導:ファイザーなど 開発中ワクチンで「抗体」量上昇を確認と発表
Phase 1/2 study of COVID-19 RNA vaccine BNT162b1 in adults
2020.7.20:英國和中國的第二期疫苗臨床試驗同日發表在刺胳針期刊
7月20日的知名期刊刺胳針(Lancet)發表了兩篇第二期臨床試驗結果,一個是牛津和英國藥廠阿斯特捷利康(AstraZeneca)合作的疫苗,一個是中國藥廠康希諾(CanSino Biologics)的疫苗,兩者都是腺病毒為載體的疫苗。
如同美國Moderna疫苗一般,也都可以成功引發中和抗體,且副作用初步看起來似乎還比Moderna少一些呢。
牛津疫苗是在18至55歲1077位受試者,中國疫苗則是508位受試者,有包含大於55歲的較年長者。一個好消息是,可能只需要打一劑,但年長者可能還是需要兩劑。
同期以”令人鼓舞的結果”為標題,評論了這兩個臨床試驗結果。兩者在第28天都可以引發抗體還有T細胞的免疫反應,都沒有嚴重的副作用。
有點令人擔心的是不是全部的受試者都有測到中和抗體,英國是90%,中國是85%左右。
詳細的結果請等我念完….

牛津和英國藥廠阿斯特捷利康(AstraZeneca)合作的疫苗,第一/二期的臨床試驗
Safety and immunogenicity of the ChAdOx1 nCoV-19 vaccine against SARS-CoV-2: a preliminary report of a phase 1/2, single-blind, randomised controlled trial

中國藥廠康希諾(CanSino Biologics)的第二期臨床試驗
Immunogenicity and safety of a recombinant adenovirus type-5-vectored COVID-19 vaccine in healthy adults aged 18 years or older: a randomised, double-blind, placebo-controlled, phase 2 trial

評論:Encouraging results from phase 1/2 COVID-19 vaccine trials

2020.7.16:莫德納(Moderna)的mRNA疫苗第一期臨床試驗結果發表,第二期也完成,準備進入第三期
莫德納(Moderna)的疫苗發表在「新英格蘭醫學期刊」NEJM:An mRNA Vaccine against SARS-CoV-2 — Preliminary Report,兩個月前新聞稿只公布有八位,現在完整報告出爐,全部受試者45人都有測到中和抗體,將於7月27日展開人數達三萬人的第三期臨床試驗。
第一期臨床試驗於3月16日開始收案,距離中國的新冠病毒基因排序公布只有66天。臨牀試驗有45位18~55歲成人健康受試者參加,4月14日完成最後收案。受試者分為三組(每組15人),注射的疫苗劑量各為25微克、100微克和250微克,注射完第一劑後,相隔28天再注射第二劑。
結果顯示:
1.施打第一劑之後,在第15天全部45名臨床試驗參與者體內都產出新冠病毒結合抗體(binding antibodies)。在第29天三個組別的抗體效價(geometric mean titer,GMT)分別為40,227, 109,209,213,526。較高劑量者產生抗體也較多。
2.施打第二劑之後可以看到抗體再度衝高。在第57天三個組別的抗體效價分別為299,751,782,719,1,192,154,可以達到新冠康復者血清相當甚至更高的抗體量(81,543 到 247,768之間)。
3.使用了兩個方式來測中和抗體(neutralizing antibody ),看是否可以對抗活的新冠病毒。在注射疫苗前全部受試者都沒有中和抗體,在43天的時候中和抗體的量都和新冠康復者血清中和抗體量相當(在抗體數值分布的上半部)。第一劑之後還沒有中和抗體,因此建議須要打兩劑。100微克和250微克以PsVNA測的中和抗體量差不多,因此第三期選擇100微克的劑量。以PRNT的方法測,100微克產生的中和抗體量是康復者血清的4.1倍。
4.新冠康復者的血清是來自38個病人,其中15%臨床上是重症(需要加護病房或插管),22%是中等症。63%是輕症。康復者的血清是用同樣的抗體檢測方式。
5.抗體之外也有測T細胞的免疫反應,目前只有25微克和100微克的資料,都可以測出有CD4輔助T細胞(Th1)的反應,但沒有什麼Th2的反應。
6.副作用方面,沒有發生第四級或是嚴重的副作用(SAE),也沒有發生嚴重到必須停止試驗的副作用。超過半數的受試者出現輕、中度副作用,包括疲勞、發冷、頭痛、肌肉痠痛與注射部位疼痛。全身性副作用在第二劑注射後較常見,特別是高劑量。250微克組在第二劑之後有三人發生了第三級副作用,全部副作用都是暫時性的且自己恢復。
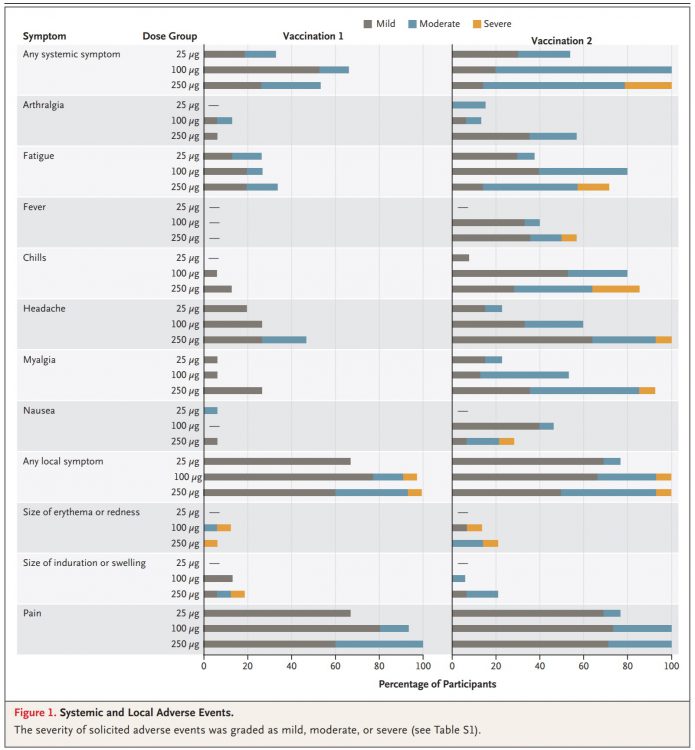
7.全身性副作用:第一劑後全身性副作用在三個組別的比例如下:33%,67%,53%。第二劑後全身性副作用比例如下:54%,100%,100%。值得注意的是,第一劑後沒有人發燒,第二劑後發燒的比例如下:0%,40%,57%。
8.局部副作用:主要是注射部位疼痛,局部紅或是腫的比例都沒有到20%。
9.有3名受試者沒有注射第2劑,其中一人是25微克組,因為雙腿有蕁麻疹;另外兩人分別為25微克組與250微克組,都因被隔離而錯過注射機會,但之後的PCR檢查皆為陰性。
結論:mRNA-1273疫苗可以在所有受試者引發抗體,沒有發生嚴重到必須停止試驗的副作用。這些發現支持這個疫苗的繼續研發。
04b解讀:
1.討論中有提到兩個對此疫苗的重要質疑。免疫力到底可以維持多久?接下來受試者會追蹤一年,看抗體還有T細胞的免疫反應後續會怎麼變化。根據之前SARS和MERS的經驗,特別是輕症患者,抗體可能不會維持很長的時間。因此這樣的追蹤非常重要。
2.第二個重要問題是之前在動物的冠狀病毒疫苗,還有SARS和MERS動物模型中都有看到的疫苗引發的肺病變。這通常和產生效果不佳的中和抗體還有引發Th2的反應有關。mRNA-1273在老鼠的實驗中就可以看到引發很好的中和抗體反應和Th1反應,可以產生CD8 T細胞防止病毒在肺部還有鼻腔增生,而沒有看到免疫傷害。現在在人體試驗看到也有產生很好的中和抗體反應和Th1反應,這個疑慮有比較減輕。
3.佛奇接受訪問時表示,對美國開發疫苗的時間表感到滿意。對疫苗來說,最重要的是他可以模擬自然感染而引發自然感染產生的免疫反應。雖然人數很少,但這就是我們看到的事情。這臨床試驗結果看起來很好,且沒有嚴重的副作用。
“The hallmark of a vaccine is one that can actually mimic natural infection and induce the kind of response that you would get with natural infection. And it looks like, at least in this limited, small number of individuals, that is exactly what’s happening. The data really look quite good, there were no serious adverse events.”
但即使疫苗成功引發免疫反應,佛奇表示,目前仍無法確定這種保護力能維持多久。這是我們目前無法回答的問題,因為疫情爆發至今只有六個月。
4.另外第一期臨床試驗還收了七個組別:50微克在18~55歲(15個受試者),年長者(56~70歲,30個受試者,25,50,100微克),還有老年人(71歲以上,30個受試者,25,50,100微克)。
還有第二期臨床試驗包括18~55歲300人,還有55歲以上300人也已收案完成(50,100微克)。以上這些資料之後也會公開。
5.第三期臨床試驗(COVE study)預計招募3萬名受試者,分為兩組,實驗組是施打100微克的疫苗,對照組則是安慰劑。預計將在7月27日開始收案,收案地點都在美國,來看受試者是否可以真正預防得到新冠感染。研究會持續進行至2022年10月27日,但初步結果應該會提早出爐。在受試者發生53個還有106個新冠感染時都會有內部分析,發生151個感染時應該就可下結論。
6.莫德納聲稱若以100微克的劑量來說,他們每年可以生產五億甚至到十億劑疫苗。
NEJM:An mRNA Vaccine against SARS-CoV-2 — Preliminary Report
STAT: First data for Moderna Covid-19 vaccine show it spurs an immune response
Moderna新聞稿:
2020.7.8 Moderna Completes Enrollment of Phase 2 Study of its mRNA Vaccine Against COVID-19 (mRNA-1273)
2020.7.14 Moderna Announces Publication in The New England Journal of Medicine of Interim Results From Phase 1 Study of Its mRNA Vaccine Against COVID-19 (mRNA-1273)
2020.5.23更新:佛奇對於莫德納疫苗的第一期臨床試驗初步結果審慎樂觀
終於等到了佛奇對於莫德納(Moderna)的mRNA疫苗第一期臨床試驗初步結果的評論。佛奇上了兩個媒體專訪,表達他受到此初步結果的鼓舞,採取審慎樂觀的態度。
Dr. Anthony Fauci says positive early results from the phase 1 study of Moderna’s Covid-19 vaccine are a good sign, “because it reached, and went over, an important hurdle in the development of the vaccine. That’s the reason why, I am cautiously optimistic about it.” #CNNTownHall pic.twitter.com/oqstmfQ6HD
— CNN International (@cnni) May 22, 2020
在星期四晚間CNN的專訪:
1.現在只有八個案例有中和抗體,似乎還是非常早期的結果,為何您會對這個結果感到鼓舞?
佛奇:在疫苗臨床試驗的路途上,有非常多可能的障礙。第一步是第一期臨床試驗,只會有非常少數的受試者,在莫德納(Moderna)的例子是收案45人,三個劑量。第一個問題是,是否安全?很明顯,他很安全。
更重要的是,發現這個疫苗可以產生中和抗體(neutralizing antibodies),而非只是結合但不知有沒有功效的抗體。在第一期臨床試驗來說,這還滿有說服力的。中和抗體是真正可以阻止病毒和人體細胞結合的抗體。 在合理的劑量下可以產生中和抗體,產生的抗體量讓我們相信在更多受試者的時候這個疫苗可以有保護力。雖然人數還不多,但產生中和抗體是非常好的消息,他達到目標且跨越了製造疫苗的一個重要障礙。這是我審慎樂觀看待的理由。
2.您已經在愛滋病病毒的疫苗努力數十年,無法產生中和抗體是否就是愛滋病病毒疫苗無法誕生的原因?
佛奇:你說的完全正確。我和同事已經在愛滋病病毒疫苗領域努力幾十年,我們的身體不會產生對愛滋病毒的中和抗體。但對於新冠病毒,絕大多數的人都是自己康復,可以產生免疫力,產生中和抗體而克服這個感染。而這也是我們在這個第一期臨床試驗觀察到的。我們總是要很小心解讀,但這是一個好消息。
在星期五早上CNBC的專訪則比較長。部分的內容和CNN類似,我就不重覆那部分。
1.在疫苗臨床試驗的路途上,有非常多可能的障礙會延長研發的時間。雖然這是漫長研發過程中的一小步,但在第一期臨床試驗的成功還是很令人鼓舞。七月如果可以順利進入第三期臨床試驗,那是一個很快速的時間。
2.為何只有八人?這些人的年齡為何?
佛奇:這是第一期臨床試驗的限制,開始一定是少人數,且是完全健康的受試者。18~45歲,我不能和你說。只能說就是這個年齡範圍,且是健康的受試者。之後較大型的臨床試驗會在老人,小孩都有受試者。
3.本週也看到中國的康希諾生物股份公司(CanSino Biologics, China)完成了第一期臨床試驗發表在Lancet,還有英國牛津大學新冠候選疫苗在動物試驗結果等等,您對於新冠疫苗會問世的信心有無改變?
佛奇:在疫苗史上,總是有許多失敗,因此我偏向保守看待。但這次世界各國有好幾個候選疫苗一起在走,我看到許多有信譽的疫苗公司,有國家的支持,我認為在我說過的12~18個月之內可以產生安全和有效的疫苗。這是我在一月開始這個疫苗研發時說的,如果我們沒有遇到意外的挫折,我們可能會在2020年12月底就可以有新冠疫苗。當然不能保證一定會有,但我保持審慎樂觀。
4.有可能有不只一個疫苗成功嗎?
佛奇:我很希望如此!你一定會希望很多疫苗能成功,若真的如此,我們會去看疫苗可能也有不同的狀況,比方說有疫苗比較適合年長者注射,有些疫苗比較適合年輕人注射。
5.對於莫德納公司這麼早公布資料方式的看法?
佛奇:莫德納自己看了初步資料,對其很樂觀而公布了。但最後NIAID會投稿在醫學期刊上,讓所有人都能檢視。
影片後面是談到美國的重新開放,瑞德西韋,還有最近佛奇自己的身體狀況。
報導:
Fauci ‘cautiously optimistic’ about Moderna’s experimental coronavirus vaccine
Fauci says it’s still possible that a coronavirus vaccine will be available in the U.S. by December
延伸閱讀:
中國新冠肺炎疫苗人體試驗結果 美專家態度保留

2020.5.21更新:星期一莫德納(Moderna)的第一期臨床試驗初步結果公布後,股價應聲大漲24%。但隨後5月19日因為波士頓環球報旗下媒體STAT的一篇文章,又讓股價重挫,宛如坐雲霄飛車。
這篇文章是由資深感染症記者布蘭威爾(Helen Branswell)採訪一些疫苗專家,指出對於目前的結果應該持保留態度不可盡信。主要有以下五點質疑:
1. 合作官方單位NIAID的沉默
美國國家過敏與傳染病研究院(NIAID)和莫德納合作開發此新冠病毒疫苗,NIAID的科學家選定了此疫苗原型,並執行臨床試驗。本周莫德納公布的初步結果便是出自此第一期的臨床試驗。但一向不低調的NIAID,不但沒有新聞稿,也拒絕對莫德納的聲明做評論。
2.僅有8人有中和抗體?
45名受試者,其中8名受試者有產生中和抗體,剩下37人的實驗結果目前未知。這不代表剩下的人沒有中和抗體,因為測試中和抗體的流程非常耗時且一定要在生物安全等級三的實驗室執行,目前只有8人的結果。目前解讀此結果還是要小心,比方說,受試者年紀分布是18~55歲,莫德納也沒公布這8人的年齡。如果這8人都偏年輕,可能抗體生成的效果會比年長的人好。而這個疫苗較重要的指標應該是要在致死率較高的年長者產生抗體。
3.不知抗體可以存在多久
目前測到的抗體是在受試者接受疫苗兩週後的資料。約翰霍普金斯大學疫苗研究人員杜冰(Anna Durbin)表示,這實在太早了,我們不知道這些抗體會維持多久。
4.抗體比較的標準是感染康復者?
新聞稿中說,疫苗所誘發抗體和新冠感染康復者的血清抗體量大致相同或是明顯超過期數值。耶魯大學的疫苗研究人員羅斯(John “Jack” Rose)表示,康復後的新冠抗體量可以差異懸殊,和疾病嚴重度可能有關。在一個175人的研究中,有10人甚至測不到中和抗體。而光譜另一邊的人則有非常高量的抗體。所以當你說基準是新冠感染康復者時,其實不確定你比較的是什麼。
而當《Stat》向莫德納詢問抗體的比較基準時,莫德納回應:這些資訊會在後續期刊發表中公佈。
5.莫德納公佈實驗結果的方式
莫德納目前為止沒有任何一個疫苗上市,但已經有數個疫苗在其生產線上。可是,莫德納其他疫苗的實驗結果也沒有在科學期刊中刊出,都像這次一樣是在新聞稿中公布。這對於科學界來說是難以信服的。
杜冰說,「他們目前為止沒有發表在新聞稿中公布的任何實驗結果,確實讓人在意。我會抱持樂觀但審慎的態度來看待。我想要看到數據,並且自己對數據進行解讀。但我認為,光是人體對RNA疫苗產生免疫反應,就是令人鼓舞的結果,因為這是針對其他病毒的RNA疫苗所沒有看到過的。這樣的抗體是否足夠,我們現在不知道。」
04b解讀:
1.以新的基因技術想做出有效疫苗是近年的顯學,但如同我上篇和大家提醒的,這家公司很新,mRNA疫苗是個很新的技術,目前為止沒有任何一個疫苗成功上市的。未知的病毒,由未知的新技術來做疫苗,自然會有很多變數。在更大型的臨床試驗中會不會看到不在預期中的副作用,產生的抗體持久與否,是否有長久免疫記憶,是否能夠順利量產,都是要克服的重重關卡。
2.在羥氯奎寧之亂之後(雖然川普說他吃了幾週了XD),我想比較健康的態度應該是審慎樂觀來看待這些新冠的醫療進展消息。我們可以樂觀看待,但要小心求證。
3.非常期待Fauci大師對於此mRNA疫苗的發言。如果大家看到請通知我。
新冠病毒疫苗數據遭質疑:一篇報導,讓莫德納市值蒸發近30億美元
Vaccine experts say Moderna didn’t produce data critical to assessing Covid-19 vaccine

2020.5.19:美國最先進入臨牀試驗的首個候選新冠疫苗:mRNA-1273傳來好消息:第一期的臨床試驗45名受試者在注射候選疫苗後,體內全都產生了新冠病毒抗體,而且沒有明顯副作用。
這是由一家mRNA疫苗及療法開發商Moderna Inc.所研發的疫苗,此計畫得到美國國家過敏與傳染病研究院(NIAID)資助。這個疫苗的特別之處是它與傳統的疫苗研發路徑不同,不使用新冠病毒本身的某部分來製作疫苗,而是找出病毒表面的棘狀蛋白(spike protein,又稱S蛋白)的核酸序列,由實驗室生成的mRNA(信使核糖核酸)序列注射進人體做為疫苗。動物實驗顯示,注射疫苗的老鼠可以有效防止病毒在肺的增生。
第一期臨床試驗於3月16日開始收案,距離中國的新冠病毒基因排序公布只有63天。臨牀試驗有45位18~45歲成人健康受試者參加。受試者分為三組(每組15人),注射的疫苗劑量各為25微克、100微克和250微克,注射完第一劑後,相隔28天再注射第二劑。
初步結果顯示:
1.目前有的抗體資料是,25微克和100微克組的第43天資料,還有250微克組的第29天資料。(因為要看前兩個劑量沒有重大副作用,才可以給更高劑量,所以進行不同步)
2.全部45名臨床試驗參與者在注射疫苗15日時,體內全都產出新冠病毒抗體。劑量越高產生的抗體量越高。
3.在25微克和100微克組,施打第二劑之後可以看到抗體再度衝高。
4.注射第二劑的兩週後(第43天),25微克組(15人)測到的結合抗體(binding antibodies)量和新冠患者復原者的血清抗體量大致相同。
5.注射第二劑的兩週後(第43天),100微克組(10人)測到的結合抗體(binding antibodies)量明顯超過新冠患者復原者的血清抗體量。有5人還沒有資料。
6.目前有用 plaque reduction neutralization (PRNT) assays的方式測了八位受試者的中和抗體(neutralizing antibody ),看是否可以對抗活的新冠病毒。25微克和100微克組各四人。和結合抗體的資料一致,在43天的時候中和抗體的量都和新冠患者復原者的血清中和抗體量相當甚至超過。和動物實驗中產生的中和抗體量也差不多。
7.mRNA-1273看來安全耐受性佳,和同公司之前mRNA的疫苗經驗差不多。25微克和100微克組各1人發生的第三級副作用是注射處紅腫。250微克組在第二劑之後有三人發生了第三級全身性副作用,全部副作用都是暫時性的且自己恢復。沒有發生第四級或是嚴重的副昨用(SAE)。
8.根據以上資料,第二期臨床試驗會修改為50微克和100微克兩組。會根據第二期的結果來決定未來七月大型第三期臨床試驗的劑量,可能是在25微克到100微克之間。
04b解讀(寫這一段,當年做疫苗臨床試驗的甘苦都湧上心頭):
1.疫苗的第一期臨床試驗的觀察重點是安全性及耐受性,因為這是第一次用在人體(first in human),需要非常的小心觀察。因此一定是要收完全健康的自願受試者,劑量從低到高,且有任何令人擔心的副作用,很可能這個臨床試驗就宣告失敗了。
2.這個mRNA疫苗的好處是他不像傳統病毒疫苗都會包含病毒的成分,他只是改mRNA的核酸序列,成分沒有這麼不可預測,因此他的安全性是比較能預期的。也因為不用取得病毒株本身,僅要有核酸序列即可做出疫苗,這種技術才能這麼快做出來。
3.第一期臨床試驗除了安全性外,也可收集初步的抗體生成性(immunogenicity)資料。就如同這個試驗做了三種不同劑量,從而決定第二期臨床試驗應該要給予的劑量。
4.我不是很確定新聞稿中所言結合抗體和中和抗體有什麼區別。中和抗體才是真正可以抑制病毒的抗體,為何不一開始就測中和抗體呢?為何僅有8人資料就公開,怎麼不測完才公開呢?
5.要提醒的是這個結果是Moderna公司的新聞稿,還沒有投稿公布完整詳細資訊。且這家公司很新,mRNA疫苗是個很新的技術,雖然此公司在過去四年總共進行了九個疫苗臨床試驗,但目前為止沒有任何一個疫苗成功上市的。進展到最後面的也只不過是巨細胞病毒(CMV)的第二期臨床試驗。讓我們繼續看下去…..
疫苗飆速!Moderna初階臨床試驗才報喜 立即籌資拚產能
Moderna Announces Positive Interim Phase 1 Data for its mRNA Vaccine (mRNA-1273) Against Novel Coronavirus
Moderna’s Work on a Potential Vaccine Against COVID-19
2020.5.14:白宮醫學顧問佛奇:新冠疫苗不一定有效
新冠病毒奪走全球近30萬人性命,各國競相研發疫苗,不過疫苗發展是一條漫漫長路,就連有「美版陳時中」之稱的白宮醫學顧問佛奇(Anthony Fauci)都坦言,「無法保證研發出的疫苗一定有效。」
美媒CNBC報導,美國國家過敏與傳染病研究院(NIAID)主任佛奇12日透過視訊出席參議院衛生、教育、勞工和退休金委員會(Senate Health, Education, Labor and Pensions Committee)聽證會時提出警告,「無法保證研發出的疫苗一定有效。」
他如此描述疫苗研發之路的複雜性:「你以為一切都到位了,但是卻沒有出現具有保護能力的免疫反應,那最大的問題是什麼,它是否有效?」
除此之外,他也表示,許多流行病學家現在擔心,疫苗有可能產生反效果,甚至讓病毒更難纏。佛奇說過去確實有2種疫苗出現了「不理想反應」(suboptimal response),人們接種了疫苗,之後再度接觸到病毒後,發病機制反而增強,「這種情況令人擔憂,所以我們希望確保這種事不會發生。」他坦言,不確定疫苗是否有效,以及會不會產生反效果,是目前疫苗研發之路面臨的2個最大未知數。
根據世界衛生組織(WHO)統計,截至4月底,全球一共有超過100支疫苗正在研發當中,佛奇表示,一直到確定疫苗有效之前,美國都仍須試圖控制疫情。不過他也對研發結果「審慎樂觀」,「我們將會有一個候選人至少有一定程度的效果。」
2020.5.6 恐做不出新冠疫苗 ?黃立民點出疫苗需兩大關鍵
1.WHO專家日前曾警告,人類可能永遠研發不出新冠肺炎的疫苗?
答:疫苗有兩大要點,第一免疫反應要有效;第二要安全不能有免疫傷害。
第一個條件是,自然感染這個病毒後,八成到九成的人都會康復,也就是說你的自然免疫是有效的,這種疫苗比較好做。如果自然免疫沒效,那就做不太出疫苗,比方說愛滋病毒還有C型肝炎病毒, 人類對他們的免疫反應都沒什麼效果,因此一直到現在為止都做不出疫苗。
第二個條件是要安全,不能產生嚴重副作用,尤其是不能產生免疫傷害。免疫傷害就是打了疫苗後,真的去得病反而更嚴重,最有名的例子就是登革熱。登革熱曾經有個國際大廠上市疫苗,後來又撤回了。
新冠病毒的疫苗在這兩點上都有問題。和它最像的兩支冠狀病毒,自然感染以後免疫反應只能維持兩年,就消失掉了,所以我們不清楚新冠病毒有效的免疫反應可以持續多久,如果它只能持續一兩年,這個疫苗就很難做。此外,別的冠狀病毒疫苗會產生免疫傷害,這個以前也被證實。所以這個疫苗兩個問題都存在。因此真的做冠狀病毒的專家,就知道這個疫苗充滿挑戰,就不會這麼樂觀。
2.有很多人體實驗,但是否成功還不一定嗎?
答:現在所有的臨床試驗都會登記在網路上,你可以去看看,能做到第三期且能夠上市的,一百個沒有兩三個,大概成功率只有2~3%。許多疫苗在臨床試驗階段就失敗了,疫苗不是這麼好做的。
3.有可能像流感一樣每年都需要打一次嗎?
答:如果做出的疫苗免疫反應時間只能維持1-2年,那就像流感一樣啦,每年要打一次比較麻煩,流感疫苗至少沒有免疫傷害,我們現在最怕的是免疫傷害。如果好不容易做出來,但有免疫傷害,那還是不能上市。
2020.3.2 新冠病毒株變異恐影響疫苗研發,對藥物影響有限
關於病毒變異:
1.病毒變異會朝著增強傳染的效率還有致病的能力這兩個方向。
2.病毒變異的位置如果變到PCR偵測的序列,那這個PCR就會測不出來。目前全世界都很即時的追蹤病毒的序列,這可以很快的修正。
3.病毒變異如果是對疫苗針對的位置變異,這就會影響到疫苗的開發,疫苗就需要改變。
(p.s.這就會讓疫苗生產所需的時間拉更長)
延伸閱讀:對這個病有較正確的認知遠比哪裡又多了案例重要!
新冠肺炎疫情下的防疫須知 常見問題解答FAQ
2019新型冠狀病毒懶人包 戴口罩勤洗手
新冠病毒無症狀感染者懶人包 如何治療?會傳染給他人嗎?會變成帶原者一直排病毒嗎?
新冠病毒未解或是常有誤解的問題懶人包
冠狀病毒流感化?武漢肺炎疫情走向預測
新冠感染各國分年齡致死率整理 小於49歲致死率較低 小於19歲較不易染病
嗅覺味覺異常可能是感染新型冠狀病毒的重要症狀 也可以是唯一症狀
新冠肺炎兒童感染症狀 兒童多為輕症不如成年人嚴重 小於五歲嬰幼兒發生重症比例較高
英國佛系防疫的豪賭 陳時中:目前台灣沒有到那個情況 國家醫療量能無法承擔才會這樣做
專家意見
黃立民教授 新型冠狀病毒訪問共筆
張上淳教授共筆 中央流行疫情指揮中心記者會
李秉穎老師新冠病毒訪問共筆
西班牙流感 1918年流感大流行 別小看流行性感冒!
武漢肺炎發生率與致死率的國際比較 by 陳建仁副總統
治療經驗
台灣新冠肺炎COVID-19病例統計分析 by 張上淳教授
敦睦艦隊疫情 04b帶你看中央流行疫情指揮中心記者會 (4.18~)
新型冠狀病毒 武漢肺炎 COVID-19 治療經驗分享
新型冠狀病毒的抗病毒藥物治療 瑞德西韋 法匹拉韋 羥氯奎寧
瑞德西韋 remdesivir 新冠治療臨床試驗懶人包
羥氯奎寧用於新冠病毒治療懶人包 小心心律不整副作用!
小心沉默的肺炎!日本自衛隊中央病院新冠治療經驗
日本疫情
東京面臨感染爆發重大局面 東京封城?首都封鎖?
通天閣太陽之塔新冠紅綠燈 大阪府知事吉村洋文推出大阪模式
日本的新冠防疫策略 專家會議整理
日本緊急事態宣言 東京大阪會封城嗎?
鈴木直道 最年輕的北海道知事
日本新型冠狀病毒疫情懶人包 日本還能不能去?現階段可以去日本旅遊嗎?
日本武漢肺炎 新冠病毒 COVID-19流行地圖
日本旅遊回來要被隔離14天嗎?可退費嗎?何謂旅遊疫情建議等級 流行地區分級?
台灣日本南韓新冠PCR檢驗量及陽性率比較 大阪 vs 北海道
鑽石公主號郵輪新型冠狀病毒疫情懶人包 由一個香港案例傳染給至少135人的海上悲劇




東京8805間旅館比價 京都7134間旅館比價
日本訂房請參考住宿懶人包,林氏璧推薦的二十四家東京旅館,26家大阪旅館,十三家京都旅館。
訂房網站推薦Relux,e路東瀛,Booking.com,Agoda。也可先用 旅館查價網站來看是否有便宜。訂行程網站推薦KKday,KLOOK客路。
到日本上網分享器和SIM卡的問題請看過這兩篇:2023日本上網卡 SIM卡懶人包,日本行動上網分享器懶人包。
各種毒友優惠及現在的活動請見:全日本篇,東京優惠,關西京阪神優惠,九州優惠,北海道優惠,沖繩優惠。
歡迎加入林氏璧的日本自助旅遊中毒者臉書粉絲專頁,或是小狸的日本購物血拼中毒者臉書粉絲專頁,接收最新日本旅遊訊息。近期有什麼活動會在粉絲專頁置頂,LINE官方帳號:@linshibi 則會直接發送最新的優惠訊息。
RSS訂閱/ 以Email訂閱 本站,東京訊息不漏接。
本站導覽 新手第一次到本站的導覽,比較容易找到資料喔。
重要公告 即日起本部落格(包括臉書頁面/私訊/e-mail)在非公開頁面不回答日本旅遊的常見問題,請各位見諒。請一律在日本自助旅遊中毒者臉書社團中問題讓大家集思廣益。
日本/東京自助旅遊的常見問題FAQ 新手請優先閱讀。



